出血リスクをいかに考えるか
次世代抗血小板療法、抗凝固療法を望む
東海大学医学部循環器内科学教授 後藤信哉氏に聞く
抗血小板薬、抗凝固薬の進歩で、抗血栓イベントの発生は一定程度抑制できる時代に入った。一方で、抗血栓イベント発生抑制効果とは裏はらの関係にある、出血イベントリスクの増加も懸念される。今後さらなる新規抗凝固薬、新規抗血小板薬の臨床現場への登場が期待される中で、出血リスクを踏まえた治療戦略の立案も求められている。東海大学医学部内科学系(循環器内科学)教授の後藤信哉氏に、抗血小板、抗凝固療法について話を伺った。
――抗血小板療法について、抗血栓抑制効果の“ベネフィット”と出血リスクとをどのように考え、勘案すればよろしいでしょうか?
後藤氏 血小板は1つの細胞で、表面には複数の受容体、内部には活性化経路があります(図1参照)。現在用いられているクロピドグレル、新規抗血小板薬である、チカグレロル、プラスグレルも、この経路の1カ所を抑制しているに過ぎず、他の血小板の機能は残存しています。抗血小板薬は血栓イベント効果も限局的ですが、出血イベント増加効果も限局的です。エビデンスに基づいた患者集団に対する介入の可能な程度の薬剤です。
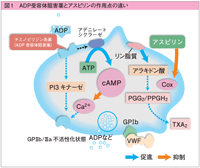
抗血小板薬が使用される病態として、冠動脈ステント留置後の血栓閉塞予防も一例です。ステント血栓症の病態を考えると、血小板よりも、血管、脂質、全身の状態、カテコラミンの増加などの血小板以外の因子の方が重要です。そのため、抗血小板薬により血栓イベントの発生を抑制できる患者の絶対数は多くありません。そう考えると、ステント血栓症発生抑制の観点から抗血小板薬が本当に必要な患者さんは、ステント治療を受けた全体からみると小さい集団と言えます。薬剤溶出ステント留置後の遅発性ステント血栓症発生率は、1000人のうち年間5人(0.5%)から、抗血小板薬の服用により、1000人のうち3人(0.3%)に抑制できるにすぎないのが実態です。これに対し、出血リスクは、抗血小板薬の服用により1000人のうち5人(0.5%)程度は重篤な出血イベントリスクを負うことになります。エビデンスに基づいた薬剤の推奨は1000例全員の服薬を勧めるのですが、本当は1000例のうち、真の意味で薬剤が必要な5例、ないし2例を選択して服用させることを考える必要があります。エビデンスを越える薬剤選択は科学ではなくて臨床医の経験に基づいたアートでしょう。
これまでの抗血小板療法は、ベネフィットも大きくないけれど、リスクも大きくないので、全員に服用させてもよい、という発想でエビデンスに基づいて患者集団に対して投与されてきました。しかし、全身のリスク管理が徹底して血栓イベントリスクが低減し、今後新規抗血小板薬のチカグレロル、プラスグレルが登場すると、患者集団全体における出血リスクが増加することも懸念されます。
投与患者の絞り込みこそが重要に
――新規抗血小板薬のリスク、ベネフィットについてはどのように考えればよいでしょうか?
後藤氏 現在、標準薬として用いられているクロピドグレルは、variability(薬効のばらつき)が懸念されており、同じ量を投与しても効果を示す人もいれば効果を示さない人もいました。
アスピリンとクロピドグレルの有効性・安全性を直接比較した、1万例規模の大規模臨床試験「CAPRIE(Clopidogrel versus Aspirin in Patients at Risk of Ischaemic Events)」の結果からも、クロピドグレルはアスピリンに比べ、血栓イベントの発生も抑制し、また出血イベントの発生率が低いことも知られています。個別の患者への薬効にはばらつきがあっても患者集団として有効性と安全性を示せれば良いというのが以前の発想でした。クロピドグレルの薬効のばらつきが科学的に事実であれば、薬効の発現しない患者では出血リスクが少ないのですから、こうした薬剤の方がEBMとして大規模集団にて有効性、安全性を示すためには有用でした。
新規抗血小板薬では、variabilityをなくすということを売り文句にしています。服薬した全ての症例に高い抗血栓効果が期待できる一方で、それらの患者は重篤な出血リスクも負うようになります。効果が強くなった時の弊害で、効果が出なくてもいい症例にも効果を示してしまい、結果として負わなくてもよい出血リスクを負うことになります。新規抗血小板薬に本当に薬効のばらつきがないのであれば、われわれ医師が真の意味で抗血小板薬を必要とする患者集団を選択して、血栓リスクの高い症例にのみ選択的に処方することを考えなければなりません。
これまでは、抗血小板薬の適応は、「一次予防」、「二次予防」などのおおまかな患者集団にて考えてきました。クロピドグレルのジェネリックが登場し、クロピドグレルの費用が圧倒的に減少する時代の到来を考えると、新規抗血小板薬の適応はさらに小集団で考えていかなければいけません。
具体的には、今後1年間に、血栓症のリスクが高い患者を絞り込み、その患者のみにコンプライアンスを保って新規抗血小板薬を服用させ、リスクの高い時期を過ぎたら安価なクロピドグレル後発品への転換を考える、ないし出血リスクとの案分において投与を中止する、などの対応です。例えば、高齢で、糖尿病や高血圧を合併、過去1年以内にイベントが起こしている…などの患者さんはリスクが高いので確実な抗血栓効果を期待した新規抗血小板薬を使うなどの対応です。服薬させる症例を限局させることにより、社会全体の出血リスクも減少することができます。次世代では、「薬剤を服用させる症例を限定する」という考えをより進めていかないといけません。
微小出血の患者長期予後は不良に
――胃腸出血、微小出血などのリスクについてはどのように考えればよいでしょうか?
後藤氏 臨床試験の結果では、頭蓋内出血が注目されがちですが、臨床家は、消化管出血や、ぶつけた所にあざができた(微小出血)なども、非常に重視します。止血するということは、血塊が血管の中にできることで、これは出血した局所だけでなく全身の血栓リスクが増加することになります。実際、「REACH Registry(Reduction of Atherothrombosis for Continued Health Registry)」の結果からも、重篤な出血イベントが起きた患者さんでは、1年以内の心血管死亡/心筋梗塞/脳卒中の発生率は出血しなかった症例の約3倍になります。頭蓋内出血では、出血そのものが麻痺につながるなどのリスクが懸念されますが、微小出血を含めて出血イベントを起こすと全身の血栓性の亢進を介して長期の血栓イベントリスクが増加すると言えます。日本人に多い「がん」も出血の1つの病態となります。「がん」による出血により抗血小板薬の投与を中止すると、血栓イベントの発生リスクはさらに高まります。日本のように「がん」の多い国では、もともと抗血小板薬は投与しない方がよかった症例も多いことになります。胃腸出血が起きた際は、患者さんの話をよく聞くと症状があるケースが多いです。稀に、顔色が白くなっている気付くケースもあります。ですから、症状がある、消化管出血の既往がある患者さんなどには、必要に応じて短期間プロトンポンプ阻害薬(PPI)の投与を考慮することも必要かもしれません。
――抗凝固療法のリスク、ベネフィットについてはどのようにお考えですか?
後藤氏 抗凝固は1つの経路しかありませんので(図2参照)、この経路を阻害した場合の抗血栓効果、出血合併症リスクは抗血小板薬より強力です。「適度な」抗血栓効果を得るためには用量調節が重要になります。その上で、血栓イベント発症予防のメリットが出血のデメリットを上回る症例を選択する必要があります。
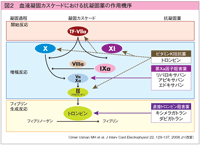
非弁膜症性心房細動の症例であれば、今後1年間に脳卒中を発症する確率が高い患者と考えると、高血圧や糖尿病を合併し、過去に脳卒中の既往があり、心エコーにて左房の著しい拡大が確認された患者など、CHADS2スコアの点数が高い患者に絞られます。新規経口抗凝固薬では出血リスクは標準化されますが、リスクが低いわけではありません。
ダビガトランでは、重篤な出血リスクは年間3%程度、日本人心房細動患者を対象にリバーロキサバンの臨床第3相試験「J-ROCKET」では、減量していても、100例のうち1例程度は頭蓋内出血を発生しています。
これだけの出血イベントリスクを負って、なおかつ将来「がん」などの出血性疾患に罹患した時には服薬を中止する必要があり、服薬中止後の短期間にはリバウンドにより血栓イベントが増加するリスクがあることまで理解して、予防的に高価な新規経口抗凝固薬を服用したいと考える症例は、私は極めて少ないと理解しています。
新規経口抗凝固薬は、臨床第2相試験の結果からも出血イベントは用量依存性に増加することが示されています。アスピリンは投与量を増加させても出血イベントは増加しません。
新規経口抗凝固薬の安全域は抗血小板薬のようには広くありません。臨床試験では、ワルファリンに比べて出血リスクが低いことが示された薬剤もあります。しかし、その結果は、あくまで、プロトロンビン時間国際標準比(INR)が2~3にコントロールしたワルファリンとの比較です。実臨床では、治験のようなプログラム化された治療は行っていません。日本の多くの臨床医は、INRが1.5、1.6でコントロールしています。INRが1.3であっても増量しないケースもありますし、逆に2.9で減量することもあります。患者さんの顔を診ながら、自らの経験にしたがって適切なワルファリン治療を行なっている実診療の出血イベントリスクは治験における出血イベントリスクよりも低いものです。私は、現在の日本のワルファリン治療が新規経口抗凝固薬に転換されると出血イベントリスクが社会全体として増加することを懸念しています。
現在、ダビガトランの投与患者は10万人と言われています。投与されている大半の症例は服用の必要のない症例です。本来であれば、脳卒中発生リスクがきわめて高い患者を選定し、それらの症例に対して「年間100人のうち、3人には重篤な出血が起こること」を説明した上で服用してもらうことが重要です。私は適切なインフォームドコンセントを行なえば、新規経口抗凝固薬の服用を希望する症例は殆どいないと考えます。ワルファリン以外の選択肢が増えたことは一部の患者には福音です。例えば、60歳でまだ会社に勤務し、3~6カ月に1度程度しか来院できないものの、家族に脳卒中の既往があり、“脳卒中は絶対に嫌だ”というような非弁膜症性心房細動患者であれば、出血リスクを説明しても新規抗凝固薬の投与対象となるかもしれません。
一方で、本当の意味で抗凝固療法が必要な70代、80代の高齢者では、2週間に1度の来院もいとわず、INRを測定した上で、ワルファリンを選択するのではないかと思います。実際、リスク、ベネフィットを説明すると、新規抗凝固薬を選択する患者は少なく、現在のところ、血栓性疾患を多く見ている私の外来でも1例を投与するにとどまっています。
「臨床試験が時代に合わなくなった」求められる臨床試験の変化
――医師としてのスキルも重視されますね。
後藤氏 実臨床は、エビデンスベースドのみで行なわれている訳ではありません。我々は、経験を重視する職人の伝統の国に生きているわけです。
EBMは、レシピに従ったファーストフードのようなものだと思います。我々の国はファーストフードよりももっとうまい職人の寿司を作ることができる国です。職人技のレシピをつくれ、といっても作れません。文章にできない部分に臨床医学のアートがあります。薬剤の添付文章、医療保険の推奨に完全には準拠しない、個別の医師の経験に応じた薬剤の用量調節、診療ガイドラインの推奨に従わない患者選択などに、医師の職人技があると考えています。
CHADS2スコアだけを見て、治療薬を選択するのであれば、経験を積んだ医師は必要ありませんよね。患者さん個人の話をよく聞いて、薬の損得勘定をよく説明して、患者さんとともに歩む覚悟のある臨床医が必要です。今日の治療方針の決定は明日変わってもいい。患者さんの要望にこまめに対応するのが良い医師だと思います。
臨床試験の数値はサイエンスなので数値でお話しますが、自分の大事な人や家族、それに匹敵する自分の患者にどのような治療を行うかは、その数値に基づいた科学で行なうわけではありませんし、製薬企業が決めた添付文書や、世界のエビデンスをまとめた診療ガイドラインに従うわけでもありません。
――臨床試験の限界が見えてきたのでしょうか?
後藤氏 むしろ、臨床試験が時代に合わなくなってきた、と言えるのではないでしょうか。循環器領域では、オンコロジーのようにゲノムレベルから薬剤を選択することができません。実臨床の経験だけでは、不満を持った患者さんや社会を説得するのが難しい中で、“適切な治療を行っている”という根拠を与えるのが臨床試験だと思います。ですから、臨床の科学としてのランダム化比較試験(RCT)は必要だと思います。
1980年代、心血管疾患の予後が悪い中で、RCTが製薬企業にとっても医師にとっても患者にとっても良いものでした。われわれはRCTの結果を踏まえ、標準治療を切り換えてきました。しかし、心血管疾患の予後が改善し、1万人を対象として数年観察しても、真のイベントが数例しか起こらない時代になって、従来型の臨床試験は行き詰ってしまいました。いま、まさに臨床試験は曲がり角に立っていると言えます。せめて1,000例程度の対象症例を集めれば仮説の検証ができるように、新薬が本当に必要な小規模の集団をいかに絞り込むか、が大切だと思います。いままで大規模なグローバル試験が仮説の検証法として注目されてきました。
しかし、グローバル試験に登録される症例には不均一性があります。むしろ、日本人には日本人の特性があります。日本人の中にも体重が50kgの人もいれば100kgの人もいる…これらの不均一性を大規模化により克服しようとした時代は終わりました。均一性の高い小規模の試験を数多く行うことが必要だと思います。
登録症例数を絞って、日本国内で試験を行なうのであれば、製薬企業の投資も少なくてすみます。企業の投資が少なければ新薬の価格を抑えることができ、医療費の削減も期待できます。
今後、ブロックバスターとなる新薬が期待できず、製薬企業が大きな投資を行うことにも期待はできません。日本の医療費は年間40超円を超えています。こうした中で今後、誰もが納得するような新薬開発のシステムが必要です。企業だけでも医師だけでも、厚労省だけでも時代の転換はできません。国民全体が主導権を握り、科学的であり、職人大国のわが国の伝統を生かした薬剤開発システムを作る必要があります。我々は日常臨床に電子カルテを使用し、日本国内は国民皆保険により均質な医療が供給されています。我が国が主導権を持って普遍性のあるシステムを構築することを皆で考える必要があります。例えば保険診療システムを活用するなどした、新たなモデルが構築されることに期待したいと思います。