バイエル薬品・イグザレルト問題 出血事象など論文掲載段階で20%超減少 本社が関与か
公開日時 2017/06/13 03:52
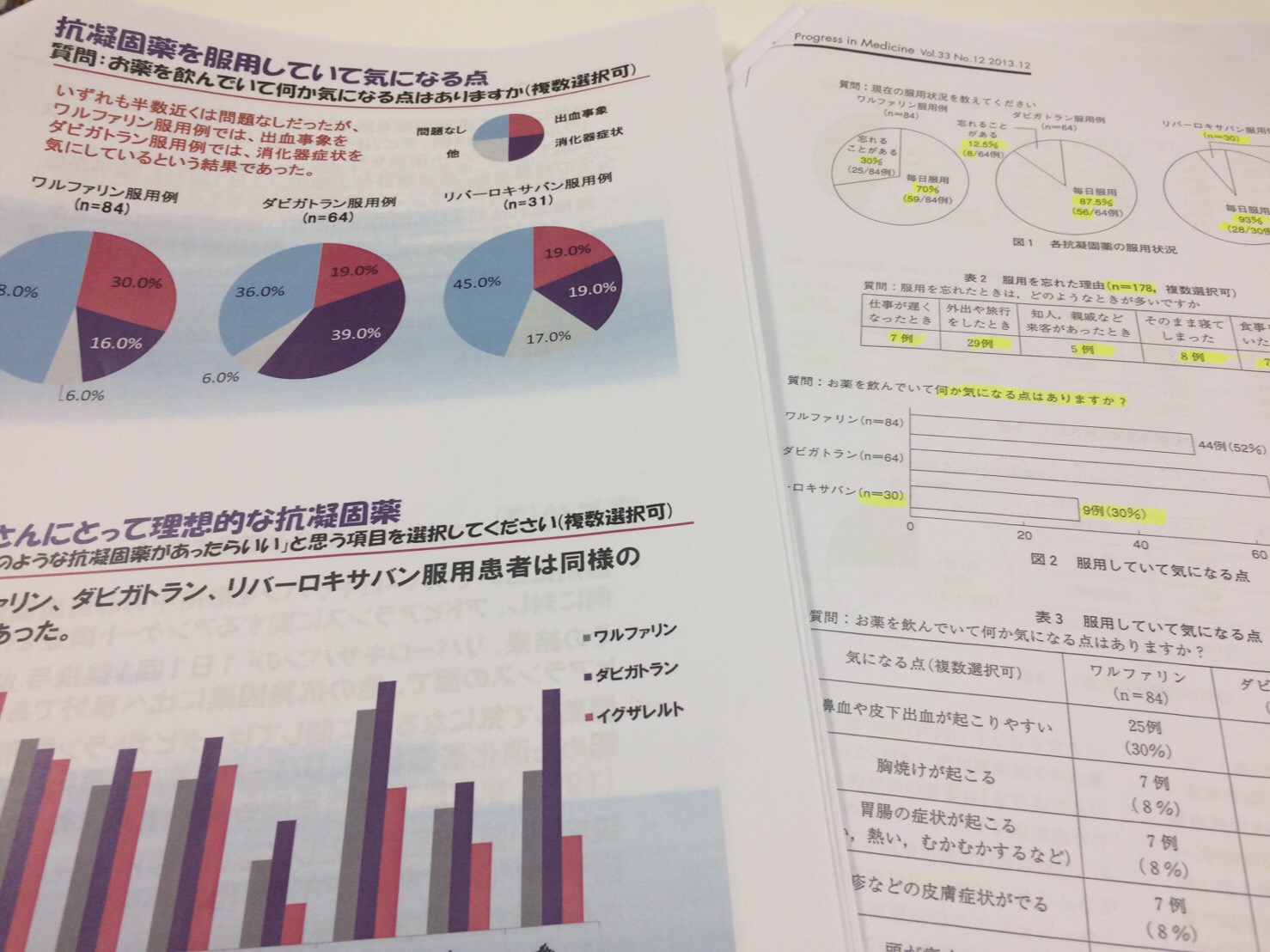 バイエル薬品の抗凝固薬・イグザレルト問題で焦点となっている宮崎県の診療所、えとう循環器科・内科で行った患者調査を検証したところ、執筆者の医師が確認した論文原稿に記載された当該薬剤の副作用報告に関するデータが、論文を正式に出版した段階で20%超減少していることが明らかになった。執筆者である江藤琢磨医師は、2013年4月に行った同剤の講演会で、イグザレルトの出血事象や消化器症状などで「気になる点がある」と回答した患者の総数を55%と報告していた。ところが同年12月に商業誌Progress in Medicineに掲載された論文では出血事象の割合が30%となっていた。本誌が入手した論文原稿は、医師の赤字が2か所の文字修正にとどまっており、データの修正はなされていなかった。
バイエル薬品の抗凝固薬・イグザレルト問題で焦点となっている宮崎県の診療所、えとう循環器科・内科で行った患者調査を検証したところ、執筆者の医師が確認した論文原稿に記載された当該薬剤の副作用報告に関するデータが、論文を正式に出版した段階で20%超減少していることが明らかになった。執筆者である江藤琢磨医師は、2013年4月に行った同剤の講演会で、イグザレルトの出血事象や消化器症状などで「気になる点がある」と回答した患者の総数を55%と報告していた。ところが同年12月に商業誌Progress in Medicineに掲載された論文では出血事象の割合が30%となっていた。本誌が入手した論文原稿は、医師の赤字が2か所の文字修正にとどまっており、データの修正はなされていなかった。
問題の論文は、2013年12月に商業誌Progress in Medicineに掲載された「抗凝固療法中の心房細動患者における服用方法の嗜好性とアドヒアランスへの影響-アンケート調査からの考察」。同論文は、バイエル薬品による資金提供が明示されており、患者調査の企画から論文の作成、掲載にいたる全ての段階にバイエル薬品本社が関与していたことも分かっている。
えとう循環器科・内科の江藤琢磨医師が2013年4月の講演会で使用したスライドのデータと、江藤医師が赤字確認した論文原稿は完全に一致していた。その一方で、同年12月に出版された論文に記載された出血事象や消化器症状などの副作用報告に絡むデータは、ワルファリンやプラザキサなどの競合品は同じ数値を掲載したが、イグザレルトに関するものだけ明らかに異なっていた。一般的に、医師の確認後に企業が数値を修正することは、倫理的、道義的に許されないこととされている。
◎出血事象などの発現を減少させるかのような印象
江藤医師が講演会で使用したスライドによると、「お薬を飲んでいて何か気になる点はありますか?」の質問に対し、イグザレルト服用例(31例)のうち55%が出血事象や消化器症状などが「気になる」と回答した。同じスライドには、ワルファリン、プラザキサなど競合薬のデータも掲載している。それによるとワルファリン服用例(84例)では52%、ダビガトラン服用例(64例)では64%と、イグザレルトの結果は、ほぼ同程度となる。しかし、この結果を12月に出版された論文に掲載されたデータと比較すると、イグザレルト投与例(30例)の副作用報告に絡む「気になる点」の回答は30%(9例)となり、競合薬2剤に比べて、出血事象などの発現を大きく減少させているような印象を与えている(写真参照)。
イグザレルトの出血事象に絡む「気になる点」を項目別にみると、「鼻血や皮下出血が起こりやすい」(記念講演会:6例→論文:4例)、「湿疹などの皮膚症状が出る」(同・2例→1例)、「頭が痛くなる」(同・3例→2例)との違いがみられる。
NOACは、脳卒中の発症抑制を主たる効能・効果とするが、一般的に出血リスクの高さが処方を阻む要因となることが知られている。ちなみに、イグザレルトの服薬状況(アドヒアランス)の良さを訴求するのに使用したデータをみると、江藤医師が使用した講演会データは「毎日忘れずに服用している」が97%(30/31例)であるのに対し、論文は93%(28/30例)と表記されていた。すでに代理人弁護士を通じ、当該診療所を担当するMRがカルテを閲覧し、EXCELにデータを記入したと証言していることから、データのダブりや何らかの記入ミスがあった可能性も否めない。ただ、30症例(n=30)のデータから副作用やアドヒアランスなどの事象を証明する場合、仮に3症例のデータを動かすだけで、その結果に10%もの差異を生じさせることを忘れてはならない。まして、この結果を製品情報概要などの情報提供ツールに使用するとなれば、情報の受け手である医師の印象を大きく左右することになりかねないのだ。
◎データのプロパティにはメディカルの名前が
本誌が入手した江藤医師の講演会スライドや論文データのプロパティには、同社のプロダクトマネージャー(当時、現・メディカル・アフェアーズ本部)の名前が記されていた。内部告発を行ったMRは、「論文の執筆は、プロマネが行った。医師の確認は1回で、2か所の修正のみだった」と証言している。医師の代理人弁護士も、「説明会資料も、論文と同様に最終確認したが、いずれもバイエル側が作成したものだ」と本誌取材に応えている。
この患者調査をめぐっては、厚労省医薬・生活衛生局の武田俊彦局長が6月1日の参院厚生労働委員会で、副作用があるにもかかわらず、9割以上のアドヒアランスを結論付けたことについて問われ、「内容が虚偽、誇大な事案にあたるかどうか予断を持たずに判断したい」と述べ、医薬品医療機器等法の66条(虚偽・誇大広告)違反に該当する可能性に言及している。
◎薬機法66条の判断は当局 バイエル薬品
バイエル薬品広報部は本誌取材に対し、「外部の専門家を 交えて本件に関する事実関係および問題の原因・背景等を徹底的に検証した上で、結果を開示 する」と問題発覚後の4月10日以降、同様のコメントを繰り返した。調査については、「患者様のカルテの一部 をデータ転記のために特定の弊社社員が不適切に閲覧していたこと、本調査の実施主体が弊社 であることについて書面上、明確にされていなかった」点について進めていると繰り返し、薬機法66条違反については「当局が判断することであり、弊社としてはお答えする立場にございません」とコメントした。