アレクシオンのソリリス 不適切プロモーションで適応外使用誘発 死亡例も多数 薬機法68条違反か
公開日時 2018/09/26 03:53
 アレクシオンファーマ合同会社の販売するaHUS治療薬・ソリリス(エクリズマブ)で、適応外使用を助長するプロモーション活動を行い、直接的な因果関係は不明であるものの、複数の死亡例が報告されていることが本誌取材で明らかになった。同社は、国内の関係学会が策定した診療ガイドとは異なる「鑑別診断の流れ」を図示した独自のプロモーション資材を作成し、MR(同社の呼称はMCC)を通じて情報提供していた。100万人に2~5人といわれるaHUSに、同社は前年比180%の目標を課し、MRに獲得症例ごとの報奨金も支給していた。医薬品医療機器等法(薬機法)第68条(承認前医薬品の広告の禁止)違反の可能性がある。
アレクシオンファーマ合同会社の販売するaHUS治療薬・ソリリス(エクリズマブ)で、適応外使用を助長するプロモーション活動を行い、直接的な因果関係は不明であるものの、複数の死亡例が報告されていることが本誌取材で明らかになった。同社は、国内の関係学会が策定した診療ガイドとは異なる「鑑別診断の流れ」を図示した独自のプロモーション資材を作成し、MR(同社の呼称はMCC)を通じて情報提供していた。100万人に2~5人といわれるaHUSに、同社は前年比180%の目標を課し、MRに獲得症例ごとの報奨金も支給していた。医薬品医療機器等法(薬機法)第68条(承認前医薬品の広告の禁止)違反の可能性がある。
◎診療ガイドと異なる鑑別診断の資材を配布
日本腎臓学会と日本小児科学会は2015年に策定した「非典型溶血性尿毒症症候群(aHUS)診療ガイド」と、アレクシオンが活用するプロモーション資材には、ソリリスの投与対象であるaHUSの鑑別診断の記載に決定的な違いが存在する。アレクシオンが18年5月に作成し、現在も使用する資材「その症例はTTPですか?それともaHUSですか?」(資材コード:HUS016-1805)には、診療ガイドで明記される「二次性TMA」の項目がない(写真参照)。すなわち「二次性TMA」もソリリスの適応と医師に誤認させるような資材を情報提供に活用させていた。
診療ガイドでは、「エクリズマブによる治療が対象となるのは、本邦の2013年の診断基準での補体制御異常によるaHUS,本診療ガイドでのaHUS(補体関連HUS)であり、二次性TMAに対する使用は現時点では推奨されない」と明記されているにもかかわらず、である。アレクシオンのプロモーション活動により、本来必要のない患者に投与されていた可能性がある。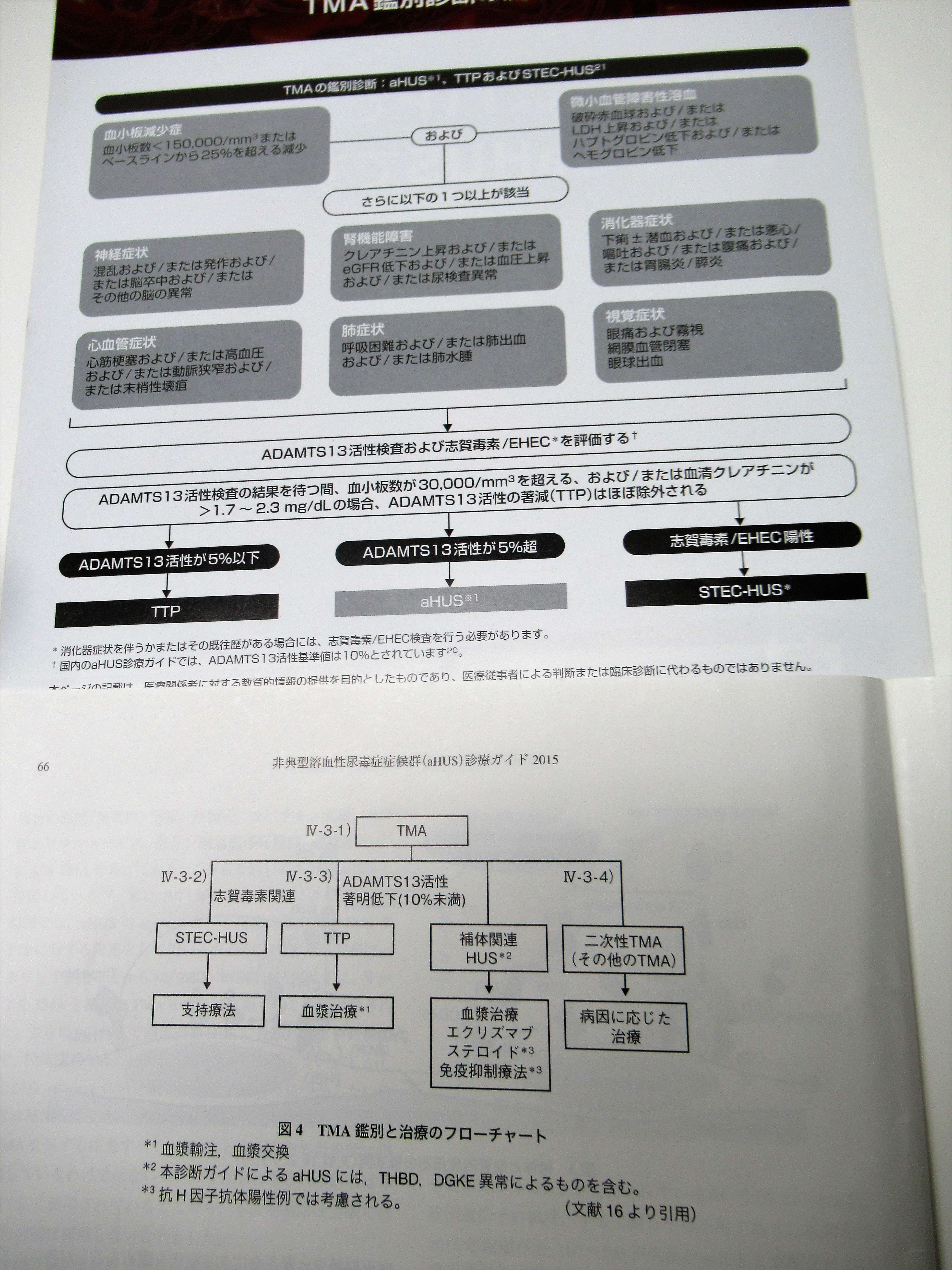
◎死亡による投与中止は31例報告 補体制御異常は3例
アレクシオンが作成した「安全性定期報告概要2018年版」によると、18年4月1日までの調査期間でソリリスを投与された解析対象症例(安全性:148例、有効性:136例)のうち、死亡による投与中止が31例報告された。このうち、ソリリスの対象となる補体制御異常とされた症例は3例にすぎず、二次性TMAが疑われる「骨髄移植・臓器移植関連」が10例など、半数以上を占めていることも分かった。
アレクシオンは安全性報告概要で、14年6月以降、「補体制御異常以外の病因分類に位置付けられるaHUS患者への投与ならびに死亡症例数は減少している」としている。ただ14年6月以降の死亡例15例でも、「補体制御異常(後天性)」は3例のみ。「骨髄移植・臓器移植関連」が3例、「感染症、薬剤性(免疫抑制薬)、骨髄移植・臓器移植関連、その他」が1例、「不明」が7例で、依然として二次性TMAに多く使用されている実態がうかがえる。なお、ソリリスは全例調査の対象となっており、同社はこうした実態を把握していたものとみられる。
◎関係学会は適正使用で注意喚起
14年6月以降に不適切使用が減少したと同社が主張したのには、日本腎臓学会が6月に、日本血液学会・日本造血結細胞移植学会が同年11月に行った注意喚起が背景にある。
なかでも日本血液学会らは、「造血細胞移植後のTMA症例の多くが極度の免疫不全状態にある」と指摘。髄膜炎菌感染症を発症するリスクがあることから、「造血幹細胞移植後のTMAに対するソリリスの安易な投与は厳に慎むべき」と注意喚起している。これら医学会の発言を踏まえ、2015年度には日本腎臓学会らが診療ガイドを改訂。「適応症ではない二次性TMAに対して本薬剤の使用が見受けられた」ことを理由のひとつにあげ、aHUSと二次性TMAを明確に分類した。18年4月には、日本腎臓学会と日本血液学会が、aHUSに限らずソリリス投与に際し、髄膜炎菌感染症のリスクがあることを注意喚起。電子カルテ上で注意喚起するなど院内の体制整備を求めている。
◎根拠論文はアレクシオンの財政的支援で作成
しかし、アレクシオンがMRを通じて情報提供するプロモーション資材の「TMA鑑別診断の流れ」(HUS016-1805、2018年5月作成)では、診療ガイドで明記されている「二次性TMA」の項目がない。aHUSはADAMTS13活性検査と志賀毒素の評価のみで鑑別診断できると誤認させる内容となっている。
この資材をめぐっては、すでに2017年夏に厚労省医薬・生活衛生局監視指導・麻薬対策課からの口頭で指導を受けているが、その後に改訂された資材は、「aHUSの定義は本邦と異なるため、国内のaHUS診療ガイド2015を参照してください」と付記したのみ。結果的に従来と同様のプロモーションがいまも継続している。このプロモーション資材の根拠とする論文「aHUS:正確な診断に不可欠な要素」(clinical advances in hematology & oncology、同社資材:ECU-REP8-1703、17年3月作成)には、「本論文にはAlexion Pharmaceuticals,Inc.の財政的支援を受けている」、「Alexionより最小限の編集サポートを得て作成した。著者は全員Alexionより謝礼を受け取っている」ことが明記されている。
 さらに18年2月の日本臨床腎移植学会で行ったスポンサードシンポジウムの記録集(18年7月作成、資材コード:HUS020-1807)には、日本人講演者の「aHUSの典型的な治療では、aHUSまたは二次性TMAと診断された場合にエクリズマブ(製品名:ソリリス)の投与を検討することになる」との発言を掲載。このほかアレクシオンの疾患情報サイトでは、同分野のKOLが、同疾患は鑑別診断には遺伝子解析検査と溶血性試験などのたんぱく解析が必要としながらも、「確定診断に時間がかかる」と述べ、検査で確定診断が出る前の急性期に同剤の投与を強く推奨していることも9月25日現在も企業サイトの中で紹介している。二次性TMAの鑑別について、国内の診療ガイドと、アレクシオンが作成する鑑別診断の流れを同じ資材内に掲載するほか、学会の診療ガイドに則った「鑑別診断のためのチェックリスト」を併せて配布するなど、内容の合致しない情報提供を行っていた。こうした状況により、厚労省や医師の目をかいくぐった可能性もある。
さらに18年2月の日本臨床腎移植学会で行ったスポンサードシンポジウムの記録集(18年7月作成、資材コード:HUS020-1807)には、日本人講演者の「aHUSの典型的な治療では、aHUSまたは二次性TMAと診断された場合にエクリズマブ(製品名:ソリリス)の投与を検討することになる」との発言を掲載。このほかアレクシオンの疾患情報サイトでは、同分野のKOLが、同疾患は鑑別診断には遺伝子解析検査と溶血性試験などのたんぱく解析が必要としながらも、「確定診断に時間がかかる」と述べ、検査で確定診断が出る前の急性期に同剤の投与を強く推奨していることも9月25日現在も企業サイトの中で紹介している。二次性TMAの鑑別について、国内の診療ガイドと、アレクシオンが作成する鑑別診断の流れを同じ資材内に掲載するほか、学会の診療ガイドに則った「鑑別診断のためのチェックリスト」を併せて配布するなど、内容の合致しない情報提供を行っていた。こうした状況により、厚労省や医師の目をかいくぐった可能性もある。
◎経営幹部「二次性TMAのなかにaHUSがいると営業を通じて医師に訴求」
ソリリスのaHUSが適応となった13年9月当時からかかわる、コマーシャルエクセレンス部の森口博史シニアディレクターは本誌取材に対し、「我々が営業の人間に言っているのは、二次性TMAのなかにはaHUSがいる可能性があるので、医師に対してそれを訴求する。判断はもちろん医師に任せる。そういうストーリーでお話をさせていただいている」と話した。
◎新薬の価値を歪める目標設定とMRへのインセンティブ 国家財政へも影響
aHUSは、国内に100万人に2~5人と言われる希少疾患だ。治療法が少ないなかで、ソリリスは医師にとっても患者にとっても、待ち望まれた薬剤と言える。一方で、ソリリスは成人1例あたり、投与開始後5回投与(29日)分の薬剤費は950万、年間の薬事費は6000万円超に上る高額薬剤だ。aHUSは2015年に指定難病に指定されており、高額薬剤であることも相まって、不適切使用があったとすれば、国家財政への影響も少なくない。
一方で、製薬企業にとっては、患者数は少ないが、一例処方させることによるインセンティブは高い。まして、マーケットサイズに見合わない前年比180%という高い目標の設定や、MRに対するインセンティブが、革新的新薬の価値を歪めた可能性は否めない。(Monthlyミクス編集部 望月英梨)